
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
ຜົນຂ້າງຄຽງແມ່ນຫຍັງ
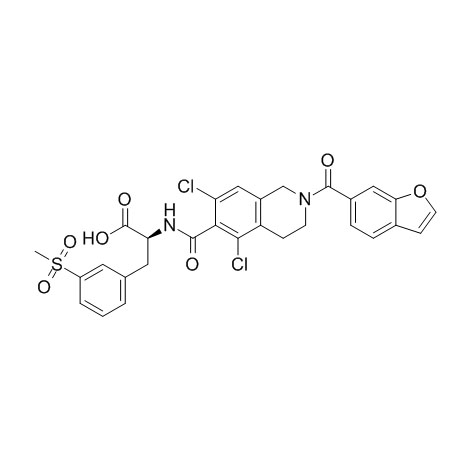
ຜົນຂ້າງຄຽງຂອງ Lifitegrast ແມ່ນຫຍັງ?
ເຊັ່ນດຽວກັນກັບຢາທັງຫມົດ, Lifitegrast ອາດຈະເຮັດໃຫ້ເກີດຜົນຂ້າງຄຽງໃນບາງຄົນ. ຜົນຂ້າງຄຽງທີ່ພົບເລື້ອຍທີ່ສຸດຂອງຢາແມ່ນການລະຄາຍເຄືອງຕາ, ເຊິ່ງເກີດຂື້ນໃນປະມານ 5% ຂອງຄົນເຈັບ. ຜົນຂ້າງຄຽງອື່ນໆທີ່ພົບເລື້ອຍລວມມີຕາມົວ, dysgeusia (ການລົບກວນລົດຊາດ), ແລະການຫຼຸດລົງຂອງສາຍຕາ. ຄົນເຈັບບາງຄົນອາດຈະປະສົບກັບປະຕິກິລິຍາ hypersensitivity, ເຊັ່ນ: ອາການຄັນ, ບາດແຜ, ແລະຕາແດງ. ຖ້າທ່ານປະສົບກັບຜົນຂ້າງຄຽງເຫຼົ່ານີ້, ທ່ານຄວນຕິດຕໍ່ກັບທ່ານຫມໍທັນທີ.
ສາມາດໃຊ້ Lifitegrast ໃນລະຫວ່າງການຖືພາໄດ້ບໍ?
Lifitegrast ບໍ່ໄດ້ຖືກສຶກສາຢູ່ໃນແມ່ຍິງຖືພາ, ແລະຄວາມປອດໄພຂອງມັນໃນລະຫວ່າງການຖືພາແມ່ນບໍ່ຮູ້ຈັກ. ແມ່ຍິງທີ່ກໍາລັງຖືພາຫຼືວາງແຜນທີ່ຈະຖືພາຄວນປຶກສາກັບທ່ານຫມໍກ່ອນທີ່ຈະໃຊ້ Lifitegrast.
Lifitegrast ປອດໄພສໍາລັບເດັກນ້ອຍບໍ?
ຄວາມປອດໄພ ແລະປະສິດທິພາບຂອງ Lifitegrast ໃນເດັກນ້ອຍຕ່ໍາກວ່າ 18 ປີຍັງບໍ່ທັນໄດ້ສ້າງຕັ້ງຂຶ້ນ. ດັ່ງນັ້ນ, ຢາດັ່ງກ່າວບໍ່ຄວນໃຊ້ໃນເດັກນ້ອຍ.
Lifitegrast ສາມາດໃຊ້ກັບຢາຢອດຕາອື່ນໆໄດ້ບໍ?
Lifitegrast ສາມາດຖືກນໍາໃຊ້ກັບຢາຢອດຕາອື່ນໆ, ແຕ່ພວກເຂົາຄວນຈະຖືກປະຕິບັດຢ່າງຫນ້ອຍ 5 ນາທີ. ທ່ານຄວນປຶກສາກັບທ່ານຫມໍຂອງທ່ານຖ້າທ່ານໃຊ້ຢາຢອດຕາອື່ນໆກ່ອນທີ່ຈະໃຊ້ Lifitegrast.
ມັນໃຊ້ເວລາດົນປານໃດສໍາລັບ Lifitegrast ເຮັດວຽກ?
ຜົນກະທົບຂອງ Lifitegrast ກ່ຽວກັບອາການແລະອາການຂອງພະຍາດຕາແຫ້ງແມ່ນມັກຈະເຫັນພາຍໃນ 2-4 ອາທິດຂອງການປິ່ນປົວ. ຢ່າງໃດກໍ່ຕາມ, ຄົນເຈັບບາງຄົນອາດຈະໃຊ້ເວລາດົນກວ່າເພື່ອຕອບສະຫນອງຢາ.
ຕ້ອງມີໃບສັ່ງຢາສຳລັບ Lifitegrast ບໍ?
ແມ່ນແລ້ວ, Lifitegrast ແມ່ນຢາຕາມໃບສັ່ງແພດ, ແລະມັນພຽງແຕ່ສາມາດໄດ້ຮັບດ້ວຍໃບສັ່ງຢາທີ່ຖືກຕ້ອງຈາກຜູ້ຊ່ຽວຊານດ້ານການດູແລສຸຂະພາບ.
ສະຫຼຸບແລ້ວ, Lifitegrast ແມ່ນຢາໂມເລກຸນຂະຫນາດນ້ອຍທີ່ໃຊ້ໃນການປິ່ນປົວພະຍາດຕາແຫ້ງ. ຢານີ້ເຮັດວຽກໂດຍການຫຼຸດຜ່ອນການອັກເສບໃນຕາແລະສະກັດກັ້ນການໂຕ້ຕອບລະຫວ່າງ LFA-1 ແລະ ICAM-1. ຢ່າງໃດກໍ່ຕາມ, Lifitegrast ອາດຈະເຮັດໃຫ້ເກີດຜົນຂ້າງຄຽງໃນບາງຄົນ, ເຊັ່ນ: ການລະຄາຍເຄືອງຕາ, ຕາບອດ, ແລະ dysgeusia. ຢາດັ່ງກ່າວບໍ່ໄດ້ຖືກສຶກສາຢູ່ໃນແມ່ຍິງຖືພາແລະເດັກນ້ອຍທີ່ມີອາຍຸຕ່ໍາກວ່າ 18 ປີ. ຖ້າທ່ານມີຄໍາຖາມຫຼືຄວາມກັງວົນກ່ຽວກັບ Lifitegrast, ທ່ານຄວນປຶກສາກັບທ່ານຫມໍຂອງທ່ານ.
ບໍລິສັດຢາ Jiangsu Run'an ຈໍາກັດເປັນບໍລິສັດຢາທີ່ມີຄວາມຊ່ຽວຊານໃນການຄົ້ນຄວ້າ, ການພັດທະນາ, ແລະການຜະລິດຢາທີ່ມີນະວັດກໍາສໍາລັບການປິ່ນປົວພະຍາດຕ່າງໆ. ພາລະກິດຂອງພວກເຮົາແມ່ນເພື່ອປັບປຸງສຸຂະພາບແລະສະຫວັດດີການຂອງປະຊາຊົນໃນທົ່ວໂລກໂດຍຜ່ານຢາໃຫມ່ແລະຄຸນນະພາບສູງຂອງພວກເຮົາ. ທ່ານສາມາດຕິດຕໍ່ພວກເຮົາທີ່wangjing@ctqjph.comຫຼືໄປຢ້ຽມຢາມເວັບໄຊທ໌ຂອງພວກເຮົາທີ່https://www.jsrapharm.comສໍາລັບຂໍ້ມູນເພີ່ມເຕີມ.
10 ເອກະສານວິທະຍາສາດກ່ຽວກັບ Lifitegrast:
1. Holland EJ, et al. Lifitegrast ສໍາລັບການປິ່ນປົວພະຍາດຕາແຫ້ງ: ຜົນໄດ້ຮັບຂອງໄລຍະ III, ແບບສຸ່ມ, double-masked, ການທົດລອງຄວບຄຸມ placebo (OPUS-3). ສາຍຕາ. 2016;123(11): 2201-2212.
2. Donnenfeld E, et al. Lifitegrast ສໍາລັບການປິ່ນປົວພະຍາດຕາແຫ້ງ: ໄລຍະ III, ການທົດລອງແບບສຸ່ມ, ຫນ້າກາກສອງເທົ່າ, ການທົດລອງຄວບຄຸມດ້ວຍ placebo (OPUS-2). ແກ້ວຕາ. 2016;35(8): 1001-1008.
3. Tauber J, et al. Lifitegrast ophthalmic solution 5% ທຽບກັບ placebo ສໍາລັບການປິ່ນປົວພະຍາດຕາແຫ້ງ: ຜົນໄດ້ຮັບຂອງການທົດລອງໄລຍະ III OPUS-1 randomized. ສາຍຕາ. 2015;122(12): 2423-2431.
4. Sheppard JD, et al. Lifitegrast ophthalmic solution 5% ສໍາລັບການປິ່ນປົວພະຍາດຕາແຫ້ງ: ຜົນໄດ້ຮັບຂອງການສຶກສາໄລຍະ III OPUS-2 randomized. Am J Ophthalmol. ປີ 2017; 177:8-19.
5. Ousler GW, et al. Lifitegrast, antagonist integrin ນະວະນິຍາຍສໍາລັບການປິ່ນປົວພະຍາດຕາແຫ້ງ. Ocul Surf. 2016;14(2): 207-215.
6. McLaurin E, et al. Lifitegrast ophthalmic solution 5% ສໍາລັບການປິ່ນປົວພະຍາດຕາແຫ້ງ: ການທົບທວນຄືນປະສິດທິພາບທາງດ້ານການຊ່ວຍແລະຄ່າໃຊ້ຈ່າຍປະສິດທິພາບ. CADTH Technol Overv. 2018;8(2): e011664.
7. Pflugfelder SC, et al. ສອງ multicenter, ການສຶກສາແບບສຸ່ມຂອງປະສິດທິພາບແລະຄວາມປອດໄພຂອງ emulsion ophthalmic cyclosporine ໃນພະຍາດຕາແຫ້ງປານກາງຫາຮ້າຍແຮງ. ສາຍຕາ. 2004;111(4): 773-782.
8. Sheppard


